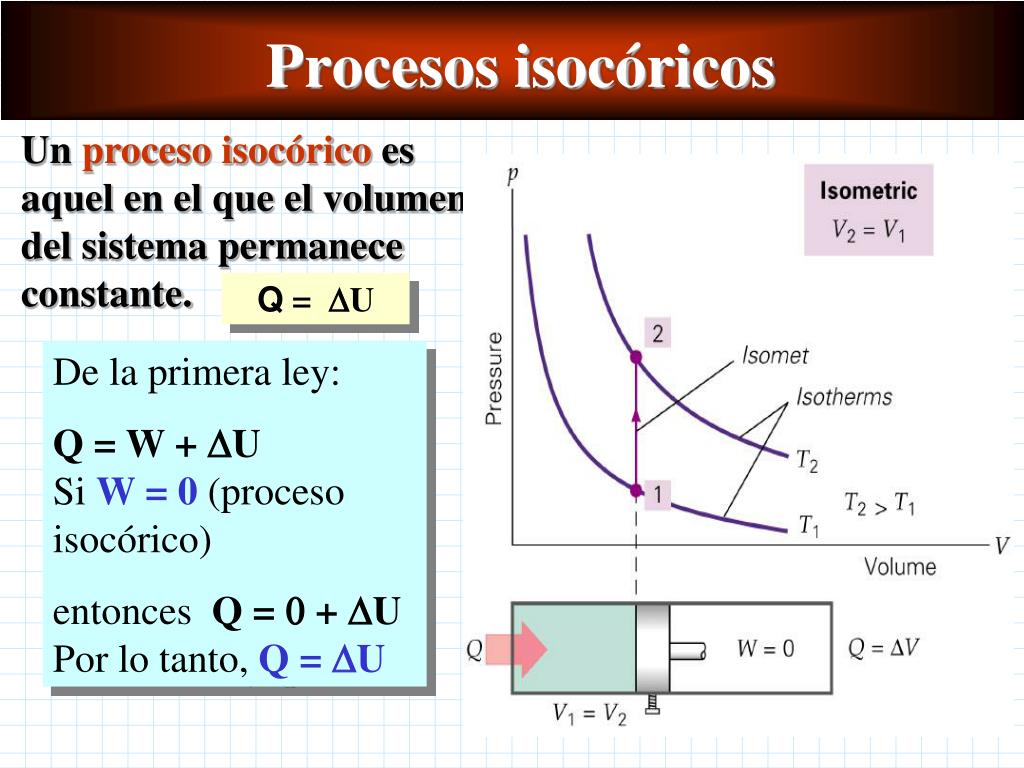
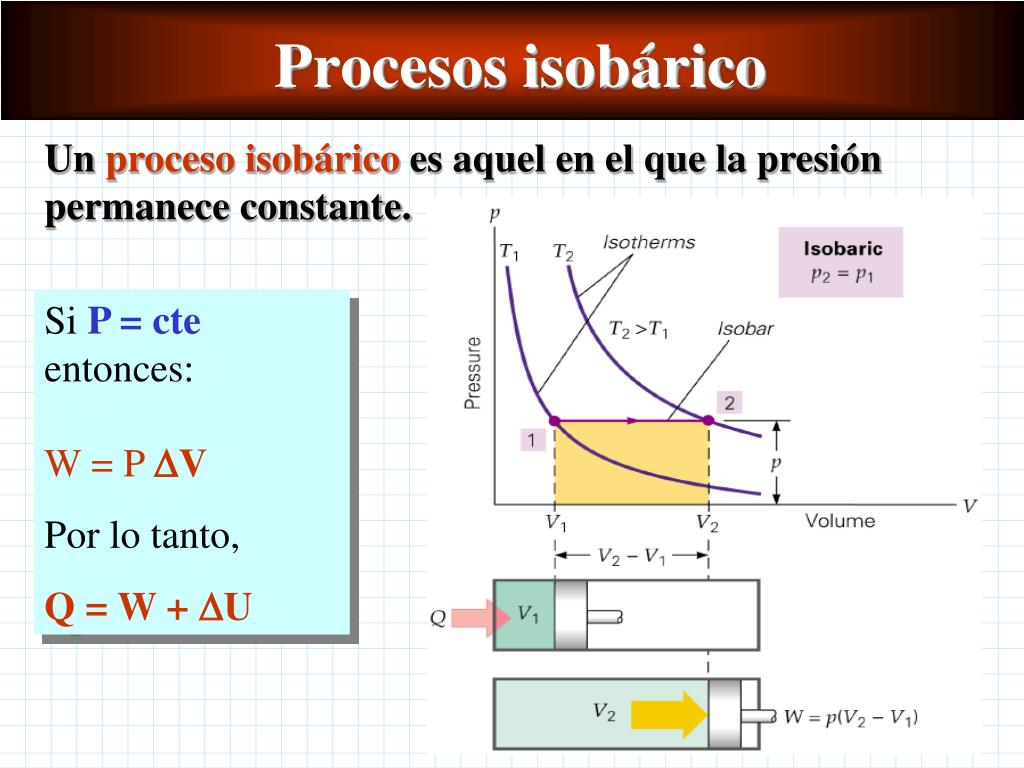
donde P es la presión (el trabajo es positivo, ya que es ejercido por el sistema).. Aplicando la primera ley de la termodinámica, podemos deducir que Q, el cambio de la energía interna del sistema es: . Q = ΔU. para un proceso isocórico: es decir, todo el calor que transfiramos al sistema quedará a su energía interna, U.Si la cantidad de gas permanece constante, entonces el incremento.. Un proceso termodinámico es cuando el calor se mueve, ya sea dentro de los sistemas o entre sistemas. Hay cuatro tipos de procesos termodinámicos idealizados: un proceso isobárico es aquel en el que la presión se mantiene constante y la temperatura y el volumen cambian entre sí. Un proceso isocórico es aquel en el que el volumen se.
PROCESO TERMODINAMICO PVT Termodinámica
PPT Termodinámica PowerPoint Presentation, free download ID6439897

Termodinámica

Termodinamica onces
PPT Termodinámica PowerPoint Presentation, free download ID5403849

PPT Unidad 5 PowerPoint Presentation, free download ID6913107
PPT Termodinámica PowerPoint Presentation, free download ID6439897

Procesos termodinámicos (Isobáricos, Isométricos, Isotérmicos y Adiabáticos) YouTube
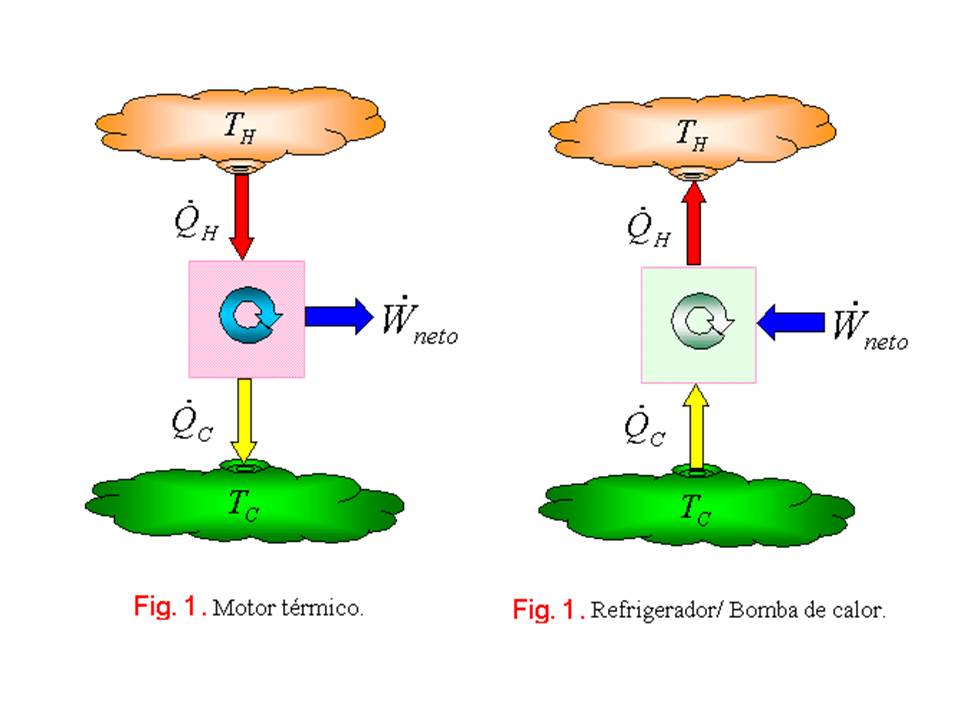
Leyes y procesos termodinámicos Primera ley de la termodinámicaConservación de la energía

CLASE 2 PRIMERA LEY DE LA TERMODINÁMICA, PROCESOS TERMODINÁMICOS YouTube

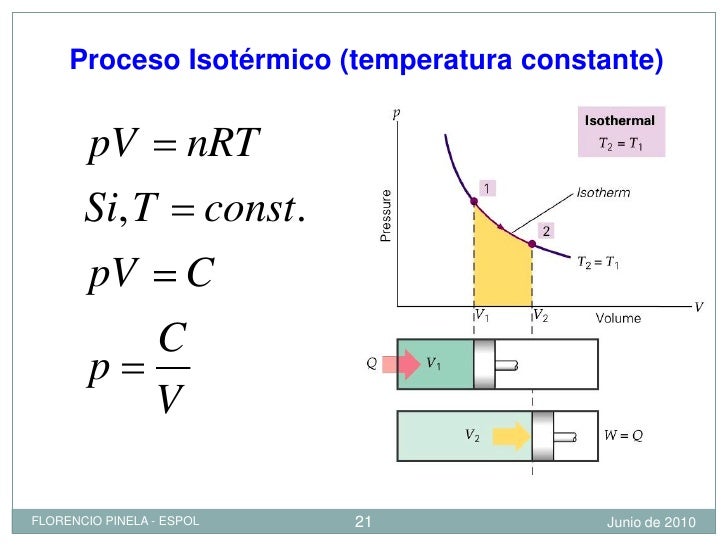
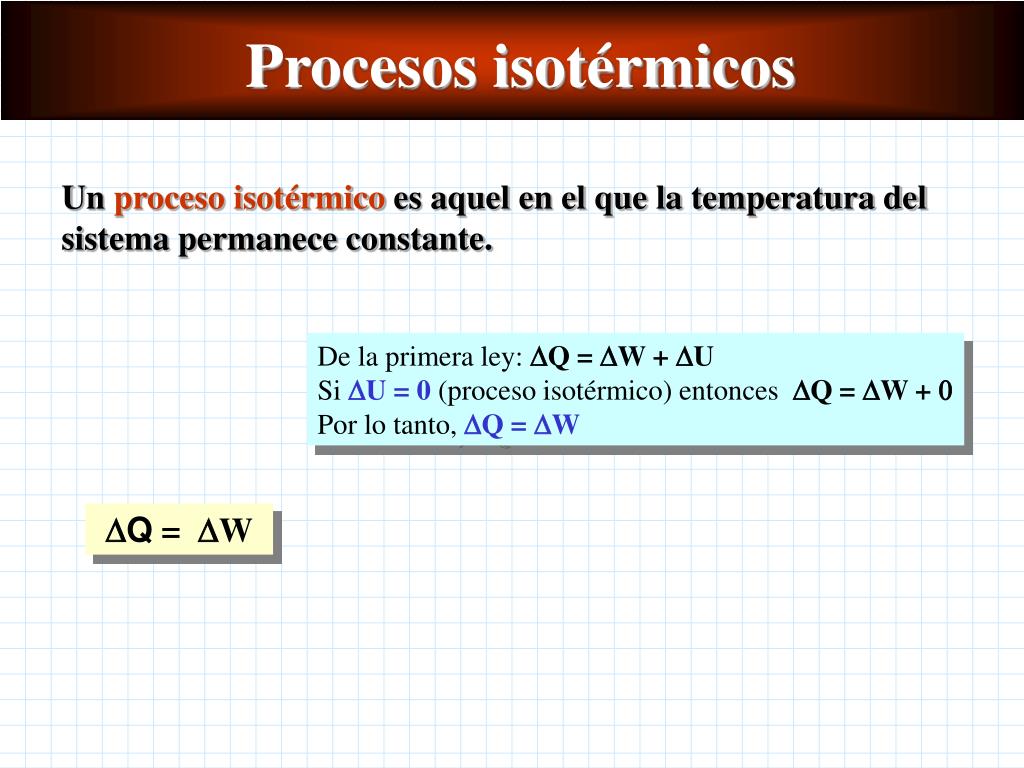
TERMODINÁMICA. CÁLCULO de la ENTROPÍA de un GAS sufriendo un PROCESO ISOTÉRMICO REVERSIBLE

Procesos termodinamicos

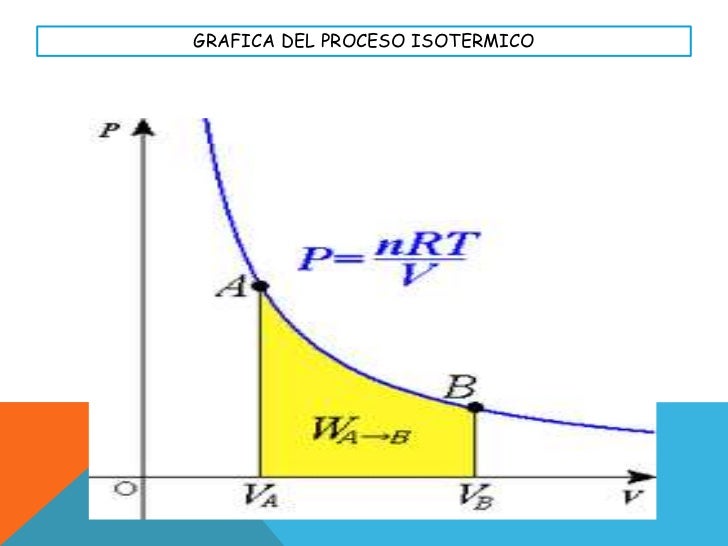
Proceso Termodinamico Isotermico

PPT Procesos Termodinámicos PowerPoint Presentation, free download ID6160861

Termodinámica Explicación del proceso ISOCÓRICO (ejemplos y aplicaciones) YouTube
Termodinamica onces

TERMODINAMICA

Proceso Termodinamico Isotermico

Cey Procesos Termodinamicos
Termodinamica
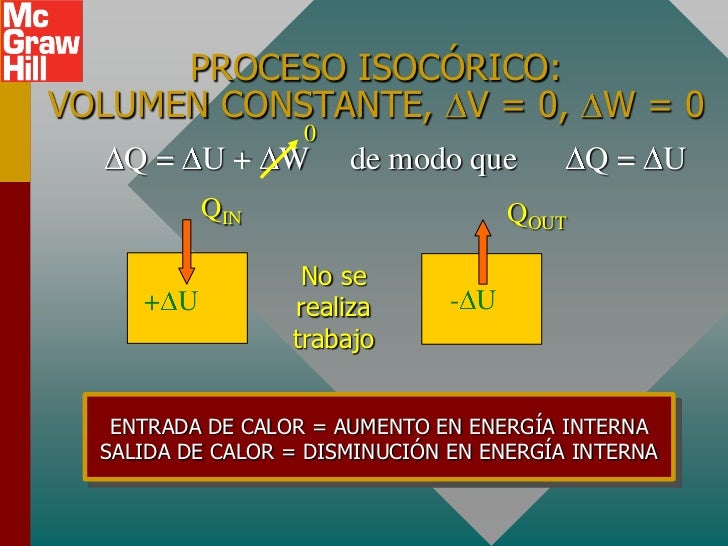
Proceso isocórico – Proceso isométrico. Un proceso isocórico es un proceso termodinámico, en el que el volumen del sistema cerrado permanece constante (V = constante). Describe el comportamiento del gas dentro del contenedor, que no se puede deformar. Dado que el volumen permanece constante, la transferencia de calor dentro o fuera del sistema no hace funcionar el p∆V , sino que solo.. El proceso isocrórico se puede expresar con la ley de los gases ideales como: En un diagrama pV , el proceso ocurre a lo largo de una línea horizontal que tiene la ecuación V = constante. El trabajo de presión-volumen del sistema cerrado se define como: Como el proceso es isocrórico , dV = 0 , el trabajo de presión-volumen es igual a cero .